Temozolomide Sandoz là gì?
Temozolomide Sandoz là một loại thuốc có chứa hoạt chất temozolomide. Thuốc có dạng viên nang (trắng và xanh: 5 mg; trắng và vàng: 20 mg; trắng và hồng: 100 mg; trắng và xanh: 140 mg; trắng và nâu: 180 mg; trắng: 250 mg).
Temozolomide Sandoz là 'thuốc gốc', có nghĩa là Temozolomide Sandoz tương tự như 'thuốc tham chiếu' đã được ủy quyền tại Liên minh Châu Âu (EU) được gọi là Temodal.
Temozolomide Sandoz được sử dụng để làm gì?
Temozolomide Sandoz là một loại thuốc chống ung thư. Nó được chỉ định để điều trị u thần kinh đệm ác tính (u não) ở các nhóm bệnh nhân sau:
người lớn gần đây được chẩn đoán mắc u nguyên bào thần kinh đệm đa dạng (một loại u não đặc biệt tích cực). Temozolomide Hospira được sử dụng đầu tiên với xạ trị, sau đó đơn độc;
người lớn và trẻ em từ ba tuổi bị u thần kinh đệm ác tính như u nguyên bào thần kinh đệm đa dạng hoặc u tế bào hình sao đồng dạng, khi khối u đã xuất hiện trở lại hoặc trở nên tồi tệ hơn sau khi điều trị tiêu chuẩn. Temozolomide Hospira được sử dụng một mình ở những bệnh nhân này.
Thuốc chỉ bán và sử dụng theo chỉ định.
Temozolomide Sandoz được sử dụng như thế nào?
Điều trị bằng Temozolomide Sandoz nên được bác sĩ có kinh nghiệm trong điều trị u não kê đơn.
Liều dùng Temozolomide Sandoz, được cho một lần một ngày, phụ thuộc vào diện tích bề mặt cơ thể (được tính bằng cách sử dụng chiều cao và cân nặng của bệnh nhân) và dao động từ 75 đến 200 mg mỗi mét vuông mỗi ngày một lần. Chúng phụ thuộc vào loại ung thư đang được điều trị, liệu bệnh nhân đã được điều trị trước đó chưa, Temozolomide Sandoz được sử dụng một mình hay với các liệu pháp khác và phản ứng của bệnh nhân với điều trị. Temozolomide Sandoz được dùng giữa các bữa ăn.
Trước khi được dùng Temozolomide Sandoz, bệnh nhân cũng có thể cần một loại thuốc ngăn nôn mửa. Temozolomide Sandoz nên được sử dụng thận trọng ở những bệnh nhân có vấn đề về gan hoặc thận nghiêm trọng.
Để biết thông tin đầy đủ, hãy xem Tóm tắt Đặc tính Sản phẩm (cũng được bao gồm trong EPAR).
Temozolomide Sandoz hoạt động như thế nào?
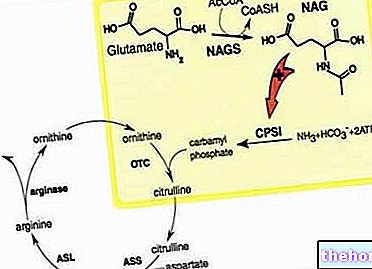
Hoạt chất trong Temozolomide Sandoz, temozolomide, thuộc nhóm thuốc chống ung thư được gọi là chất alkyl hóa. Trong cơ thể, temozolomide được chuyển đổi thành một hợp chất khác gọi là MTIC. MTIC liên kết với DNA của tế bào trong giai đoạn sinh sản, do đó ngăn chặn quá trình phân chia tế bào. Kết quả là, các tế bào ung thư không thể sinh sản và sự phát triển của khối u bị chậm lại.
Temozolomide Sandoz đã được nghiên cứu như thế nào?
Vì Temozolomide Sandoz là một loại thuốc thông thường, các nghiên cứu chỉ giới hạn ở các bằng chứng cho thấy rằng thuốc tương đương sinh học với thuốc tham chiếu, Temodal. Hai loại thuốc có giá trị tương đương sinh học khi chúng tạo ra cùng mức độ hoạt chất trong cơ thể.
Những lợi ích và rủi ro của Temozolomide Sandoz là gì?
Vì Temozolomide Sandoz là thuốc gốc và có giá trị tương đương sinh học với thuốc tham chiếu, nên các lợi ích và rủi ro của thuốc được giả định giống như thuốc tham chiếu.
Tại sao Temozolomide Sandoz được chấp thuận?
Ủy ban Sản phẩm Thuốc dùng cho Con người (CHMP) kết luận rằng, dựa trên các yêu cầu của luật pháp EU, Temozolomide Sandoz đã được chứng minh là có chất lượng tương đương và tương đương sinh học với Temodal. Do đó, CHMP cho rằng, như trong trường hợp của Temodal, lợi ích lớn hơn rủi ro đã xác định. Do đó, Ủy ban đề nghị cấp phép tiếp thị cho Temozolomide Sandoz.
Thông tin khác về Temozolomide Sandoz
Vào ngày 15 tháng 3 năm 2010, Ủy ban Châu Âu đã cấp cho Sandoz Pharmaceutical GmbH một "Giấy phép Tiếp thị" cho Temozolomide Sandoz, có giá trị trên toàn Liên minh Châu Âu. "Giấy phép Tiếp thị" có hiệu lực trong năm năm và sau thời hạn có thể được gia hạn.
Để có phiên bản EPAR đầy đủ của Temozolomide Sandoz, hãy nhấp vào đây Để biết thêm thông tin về liệu pháp với Temozolomide Sandoz, vui lòng đọc tờ rơi gói (kèm theo EPAR).
Bạn cũng có thể tìm thấy phiên bản EPAR đầy đủ của thuốc tham chiếu trên trang web của Cơ quan.
Lần cập nhật cuối cùng của bản tóm tắt này: 01/2010.
Thông tin về Temozolomide Sandoz được công bố trên trang này có thể đã cũ hoặc chưa đầy đủ. Để sử dụng đúng thông tin này, hãy xem trang Tuyên bố từ chối trách nhiệm và thông tin hữu ích.